产品单价 |
面议 |
起订量 |
1 |
供货总量 |
不限量 |
发货期限 |
自买家付款之日起3天内发货 |
FDA |
510K |
510K |
美代 |
之前美国对于医疗器械办理510K的问题真的是一波三折
2021 年 1 月 15 日,联邦公报发布通知“通过使某些医疗器械免于上市前通知要求,从而在COVID-19 公共卫生紧急事件期间提供的监管灵活性;要求对 510(k)计划的进一步科学和循证改革机会提供信息,研究,分析和公众意见
通知表明病人检查手套即刻豁免上市前通知要求,即 510(k)要求。
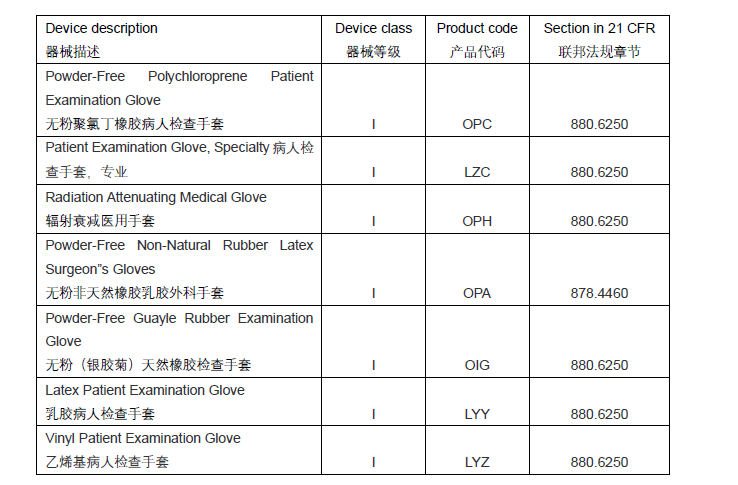
7月26日,美国卫生与公众服务部 (HHS) 和美国食品和药物管理局 (FDA) 在联邦公报中发布了一项指令,确定七种类型的外科医生手套和患者检查手套需要上市前通知 (也称为 510(k))。该命令范围内的产品代码为:LYY、LYZ、OIG、OPC、OPH、LZC、OPA
简单通俗的讲,之前的通知取消了
那我来给大家讲一下他的申请流程:我们归纳了以下三个步骤
步,根据产品确定产品的类别,识别产品代码,找到合适的比对器械,确定适用标准和检测项目。这一步是难的,很多时候FDA并没有完全列出所有标准,指导材料和表格也并不,这一步一般需要的FDA顾问来帮助企业完成。
第二步,企业根据标准和检测项目准备测试及基础资料,基础资料包括但不限于产品技术工艺资料、结构参数资料、测试数据和报告等。
第三步,FDA顾问根据法规要求和基础资料编写510(K)报告,提交申请,交由FDA相关部门审核。
其中检测是难的一部分:
手套标准
1)美标《ASTM D6319 医疗用丁腈检查手套的标准规范》全部项目、《ASTM D5250 医疗用聚氯乙烯手套的标准规范》全部项目、《ASTM D3578橡胶检查手套的标准规范》全部项目
2)欧标EN 455-1、-2、-3、-4《一次性医用手套》除生物相容性检测外所有项目
3)国标《GB 10213-2006 一次性使用医用橡胶检查手套》《GB 24787-2009一次性使用非灭菌橡胶外科手套》部分检测项目
武汉沙格对于手套510K申请经验丰富,成功案例诸多,后续有相关认证检测可以随时联系
| 武汉沙格医疗科技有限公司 | |||
|---|---|---|---|
| 联系人 | 蒋梦蕾 |
微信 | 18007141921 |
| 手机 | | 邮箱 | 2997246458@qq.com |
| 传真 | 无 | 地址 | 新华西路武汉菱角湖万达广场A3座1206 |
| 主营产品 | 欧盟ce美国fda,英国ukca,FDA510K,检测咨询 | 网址 | http://sungo18007141921.b2b.huangye88.com/ |




